文部科学大臣賞
エサ条件によるプラナリアの成長と自切に及ぼす影響
![]()
佐藤 大悟
- 東京都荒川区立第四峡田小学校 4年
佐藤 大悟 -
第66回入賞作品
小学校の部
文部科学大臣賞
研究のきっかけ
目の不自由な方と交流する機会があった。目が見えないことで生じる困りごとを少しでも減らしたいと思い、カメラを搭載した白杖を開発した。その白杖には、カメラで撮影した文字を読み上げる機能がある。けれども、ものに頼らず、目の機能そのものを再生できたらどんなに喜ばれるかと思った。そんな時、「免疫ふしぎ未来2024」という科学イベントで、プラナリアという無脊椎動物を5匹いただいた。プラナリアは三岐腸目に属する体長1cm前後のナミウズムシの一種だ。川などに生息し、岩や石の下など暗所を好む。高い再生能力を持ち、体が切断されてもそれぞれの断片が再生して、個体が増える。「免疫ふしぎ未来2024」でいただいた5匹のプラナリアも、飼育するうち1000匹に増えた。プラナリアの再生の仕組みを学べば、人間の失われた機能の回復に役立つかもしれないと考えて、この研究を始めた。
プラナリアの生態
プラナリアの体の特徴は、次のようなものだ。
眼点は18°に傾いていて、光しか感知しない。プラナリアは光を避ける行動をとる。耳葉は聴覚器官ではなく、水中のにおいや味を感じる感覚器官である。食事をする時は咽頭から管を出す。排泄物も咽頭から出している。体表はじゅう毛と粘液で覆われている。腸は3つに分かれていて、血管がないため腸が体のすみずみまで栄養を届ける働きをしている。
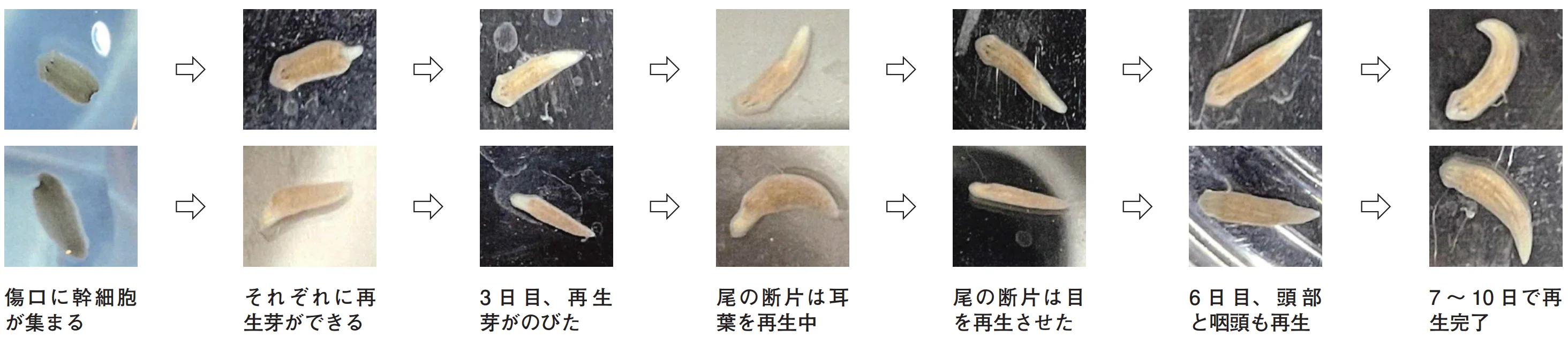
プラナリアは、自切と呼ばれる無性生殖をする。自分で体をちぎり、ちぎれた断片がそれぞれの個体へと再生する。自切ではまず、体の一部が細くくびれる。体の中央よりやや尾側がくびれることが多い。次に頭と尾に分かれるが、最後は自らの消化液で切り離す。自切後の断面は滑らかで、人工的に切断した場合(断面が整わず体液が多くもれる)とは違う。前後に分かれた頭部と尾部はそれぞれ新しい尾部と頭部をつくって、7〜10日前後に再生する。頭部も尾部も、再生の途中で動き始める。今回の観察では、尾部から頭部をつくって再生するほうが日数がかかった。頭部の脳神経や感覚器官を再生するのに、時間がかかったと考えられる。
プラナリアの自切から再生まで
上の段が頭の断片、下の段が尾の断片
研究の目的
プラナリアが日常的に食べているエサが、再生能力にどう影響しているのか、知りたいと思った。プラナリアが摂取するエサの違いで、自切の回数や個体数の増え方が変わるのか、よくわかっていない。
プラナリアに赤虫と豚のレバーという異なるエサを与えて、自切の回数、個体数の増え方に違いが出るのかどうか、実際に確かめることにした。
研究①〜②
研究①では、飼育しているプラナリア20匹で実験を行った。プラナリア20匹を1週間絶食させた後、10匹ずつの2群に分けて飼育シャーレに入れた。片方にはエサとして研究でよく使われる豚レバーを与え、もう片方にはエサとして自然界に近い冷凍赤虫を与える。2つの群で自切の起こり方に違いがあるか、観察した。
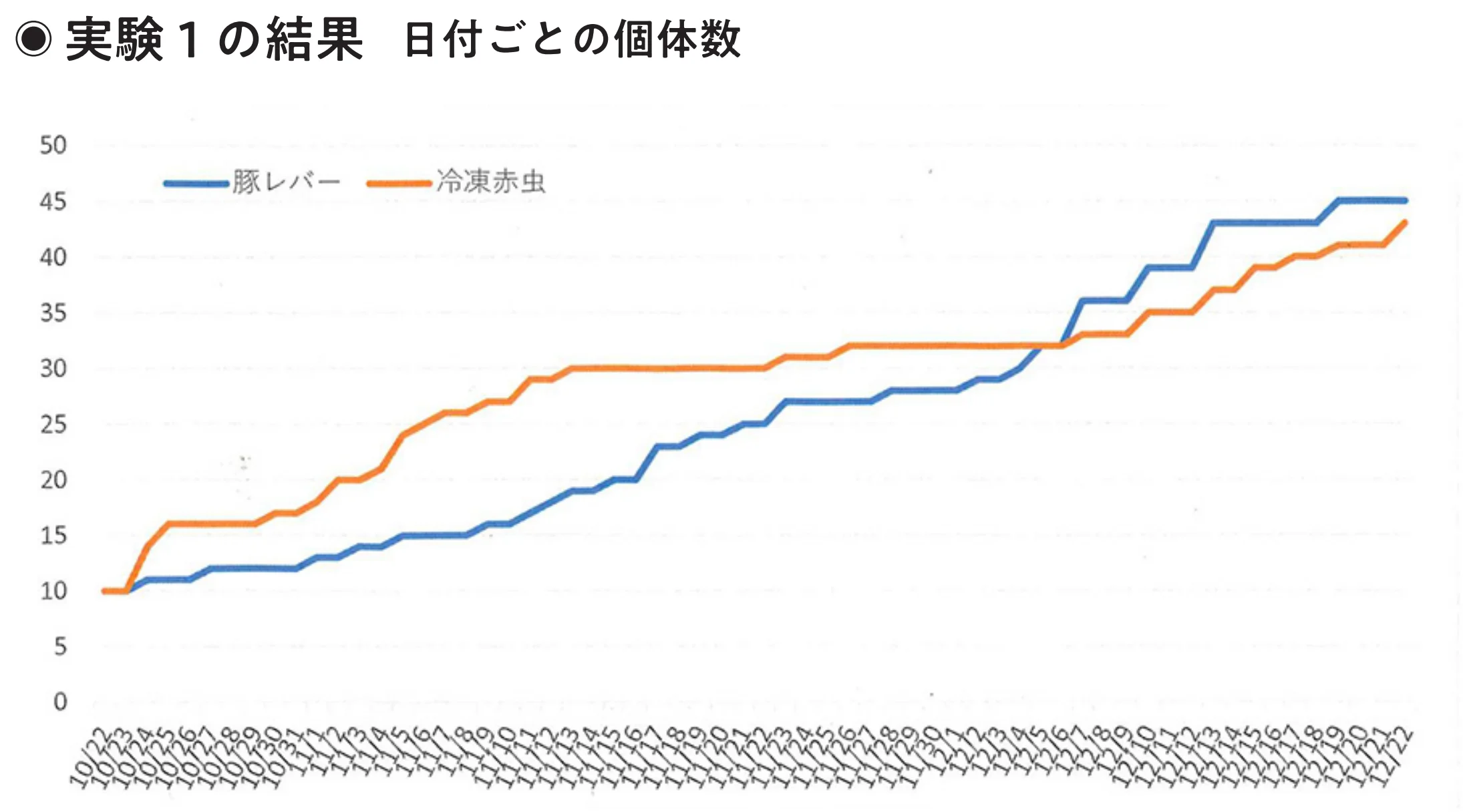
実験1
2つのシャーレにはカルキ抜きした水道水を入れ、水は毎日交換した。水温は21℃前後を保つようにする。エサは3日に1度、17時から3時間ほど与えて全匹満腹になるようにし、残ったエサはすべて取り除く。2024年10月22日から12月22日まで観察し、自切の有無と個体数の変化を毎日記録した。
実験前の予想では、赤虫群のほうが自切の回数は多いと思った。赤虫は川や池に生息するユスリカの幼虫で、自然界に近いエサである。プラナリア本来の生態に合った栄養や刺激を与えることで、活発に自切が起こるのではないかと予想した。
実験の結果は、上のグラフのとおりだ。自切の回数は予想とは違い、豚レバー群のほうが多かった。11月下旬までは赤虫群のほうが多く自切していたが、12月に入ると豚レバー群の自切が増加した。12月22日の最終日までに豚レバー群が10匹から45匹、赤虫群が10匹から43匹に増えていた。
豚レバーには脂肪やビタミンが豊富に含まれ、短期間で体が大きくなりやすいため、多くの自切につながったのかもしれない。自然界のエサに近い赤虫はたんぱく質を多く含むため、赤虫群には安定した成長傾向が見られた。2つの群の違いはエサが影響した可能性もあるが、同じ群でも個体によって自切のタイミングや回数に差があった。エサ以外に、個体の体質の違いが影響しているのかもしれない。そこで、より信頼性を高めるため、観察する赤虫を増やした追加実験をすることにした。
実験2
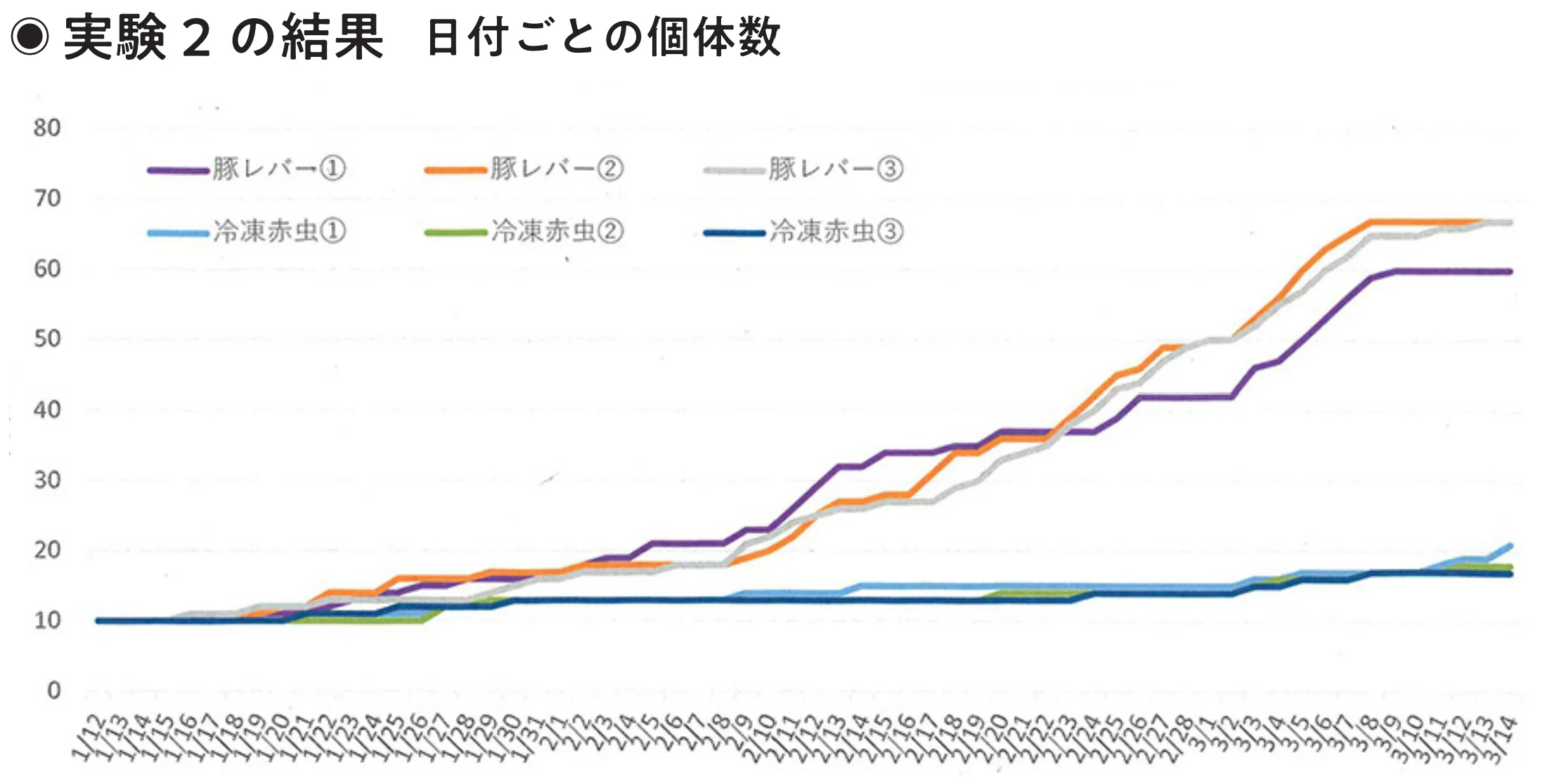
実験1と同じプラナリアを使い、同じ方法で行うが、最初の個体数を60匹へ増やした。30匹ずつ2群に分け、各群10匹ずつ3つのシャーレを用意、合計6つのシャーレで観察した。観察期間は2025年1月12日から3月14日までだ。実験1と同じように、最終的には豚レバー群が多く増えると予想した。観察の終わりには、1シャーレ50〜60匹になると期待する。
実験の結果は、左下のグラフの通りだ。赤虫群は1〜2月は個体数の変化が少なく、3月に入ってから少しずつ増加したが、最終的に17匹、18匹、21匹と微増レベルにとどまった。豚レバー群は2月初めまでほとんど変化がなかったが、その後は急に増え始め、3月に50匹を超えると最終的には60匹、67匹、67匹となった。赤虫群は体長12mm以上を保つ個体が多く、豚レバー群は8mm前後の小さい個体が多くなるのも特徴的だった。両群の増え方の違いは、エサに含まれる栄養素の違いと推測できるため、冷凍豚レバーと冷凍赤虫に含まれる栄養素も調べてみた。
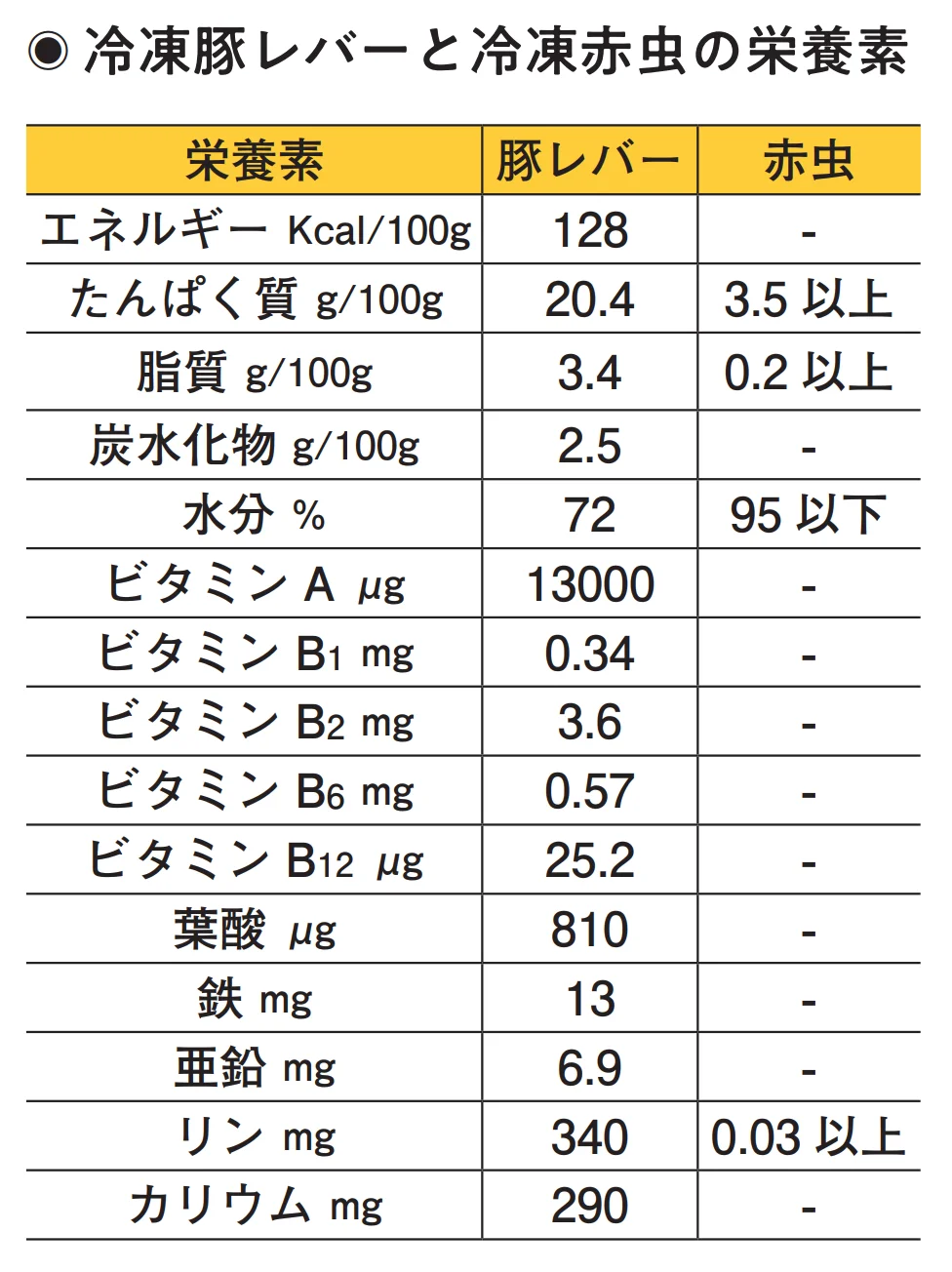
すると冷凍豚レバーにはたんぱく質に加え、ビタミンAや鉄分など多くの栄養素が含まれていた。冷凍赤虫は水分が多く、栄養素は少なめだった。2つのエサの栄養素の違いが自切の回数に影響し、個体数の差になったと考えられる。自然界のプラナリアは水生生物を食べるため、豚レバー群のように栄養価が高いエサを食べる機会は少ない。赤虫群の増え方が自然界の生態に近いといえるが、豚レバー群の結果は摂取する栄養素によってプラナリアが個体数を大きく増やせる可能性を示している。栄養素の影響をさらに詳しく確かめるため、与えるエサを既存のものとは替え、増え方がどう変化するかも確かめてみる。
研究③〜④
実験3
実験3は、豚レバーだけを与えた群、赤虫だけを与えた群から合計40匹を選んで使った。40匹のプラナリアをA〜Dの4群に分け、4つのシャーレで飼育する。A群はもともと冷凍赤虫を与えていたプラナリアで、この実験では冷凍豚レバーを与える。B群はもともと豚レバーを与えていたプラナリアで、この実験では赤虫を与える。C群はもともと豚レバーを与えていたプラナリアで、今回も豚レバーを与え続ける。D群はもともと赤虫を与えていたプラナリアで、今回も赤虫を与え続ける。
実験方法は実験1〜2と同じ、2025年2月11日から5月11日まで、各群の個体数と、それぞれの体長を記録した。
実験を前に、最も個体数を増やすのは豚レバーだけを与えるC群、次いでB群、A群と続き、最も少ないのは赤虫だけのD群という予想を立てた。ところが実際は、最も個体数を増やしたのは赤虫から豚レバーへエサを切り替えたA群だった。3月10日に50匹に到達し、最終日には210匹となった。次いで多かったのは豚レバーから赤虫に切り替えたB群、4月6日に51匹に到達し、最終日には93匹となった。最も多いと予想していた豚レバーだけのC群は76匹までしか増えず、急激な増加は見られなかった。赤虫だけのD群は予想どおり最も少なく29匹までの増加で終了したが、他の群のプラナリアが体長8mm前後なのに対し、12mm前後の際立って長い個体が多かった。
この体長の違いをよりわかりやすく示すため、各群10匹ずつの体長測定値をもとにバイオリンプロットを作成した。D群は最も体が長く、個体ごとのばらつきが少ない。反対にC群は体が短い個体が多く、ばらつきも大きい。これは栄養価の高いレバーを食べることで短い体長のまま自切がくり返され、個体差が大きくなるためだと考えられる。途中でエサを替えたA群とB群も、すぐに体長は回復せず、豚レバーの影響が続いているように見える。この実験から、エサの違いが体の大きさにも影響することが、わかってきた。実験4ではA〜D群それぞれの自切の様子をさらに詳しく、個別に観察することにした。
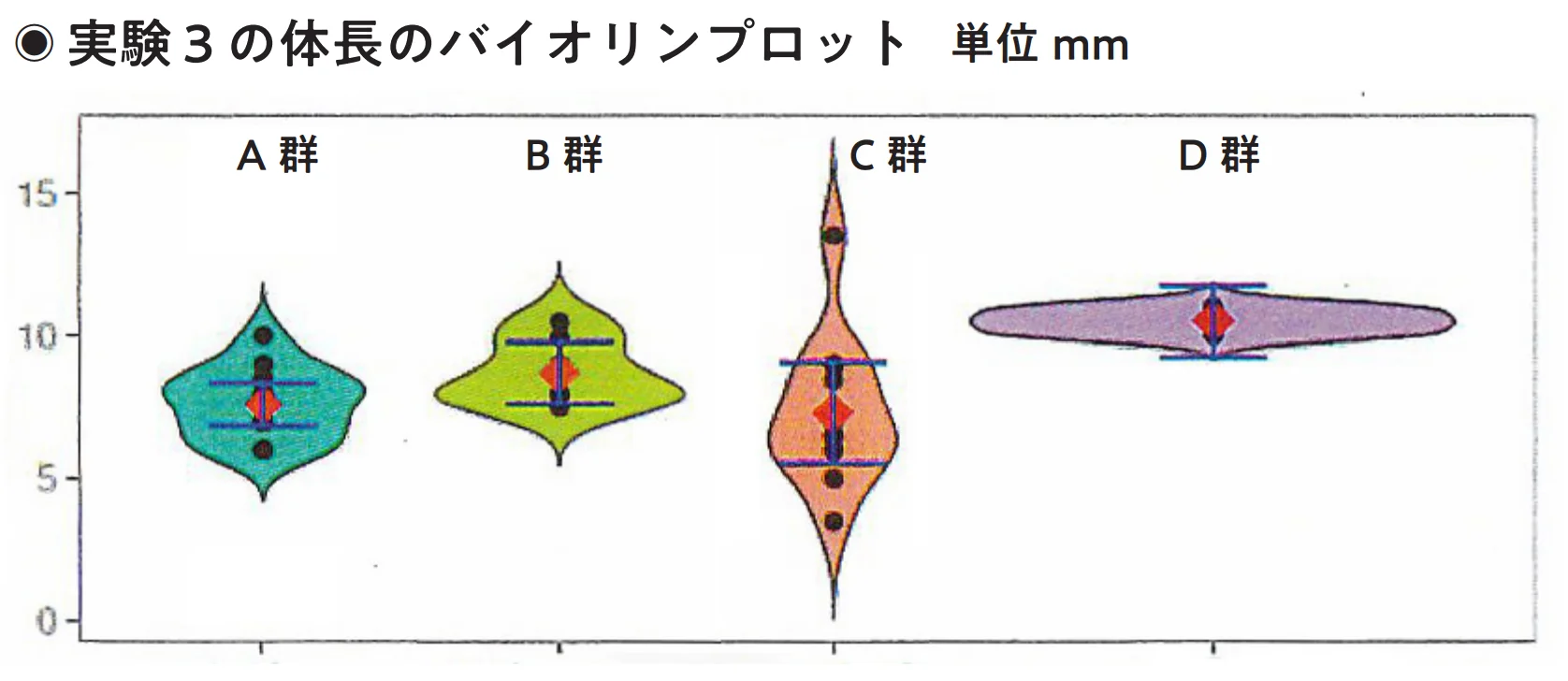
左から「赤虫→豚レバー」「豚レバー→赤虫」「豚レバーだけ」「赤虫だけ」のバイオリンプロット、中央の黒い点は実際に測った個体の体長データ、赤い菱形は平均値、青い線はデータのばらつき幅、左右に広がる曲線はその体長の個体数を表し横に広い部分ほどその長さの個体が多いことを示す
実験4
実験3のA〜D群からそれぞれ3匹ずつを選び、12穴プレートに1匹ずつ入れて、他の個体と接触しないようにしながら観察した。水はカルキ抜きした水道水を使い、毎日交換する。冷凍豚レバーと冷凍赤虫をエサにすることなどは、実験3と同じだ。2025年3月28日から7月28日まで毎日19時に観察し、自切が起こった日や回数、体長を記録する。最初の12匹の個体には、あらかじめ1〜12の番号を振った。例えば1番の豚レバーだけを与えていたプラナリアが自切した場合、2つの断片をあらかじめ用意した新しい12穴プレートに移して1-1、1-2と番号を振り、それぞれ同じエサ(この場合は豚レバー)を与えて同条件で観察を続けた。再生した1-1が自切した場合も2つの断片を違う穴に移し、1-3、1-4というように番号を振り、同条件で観察を続けた。
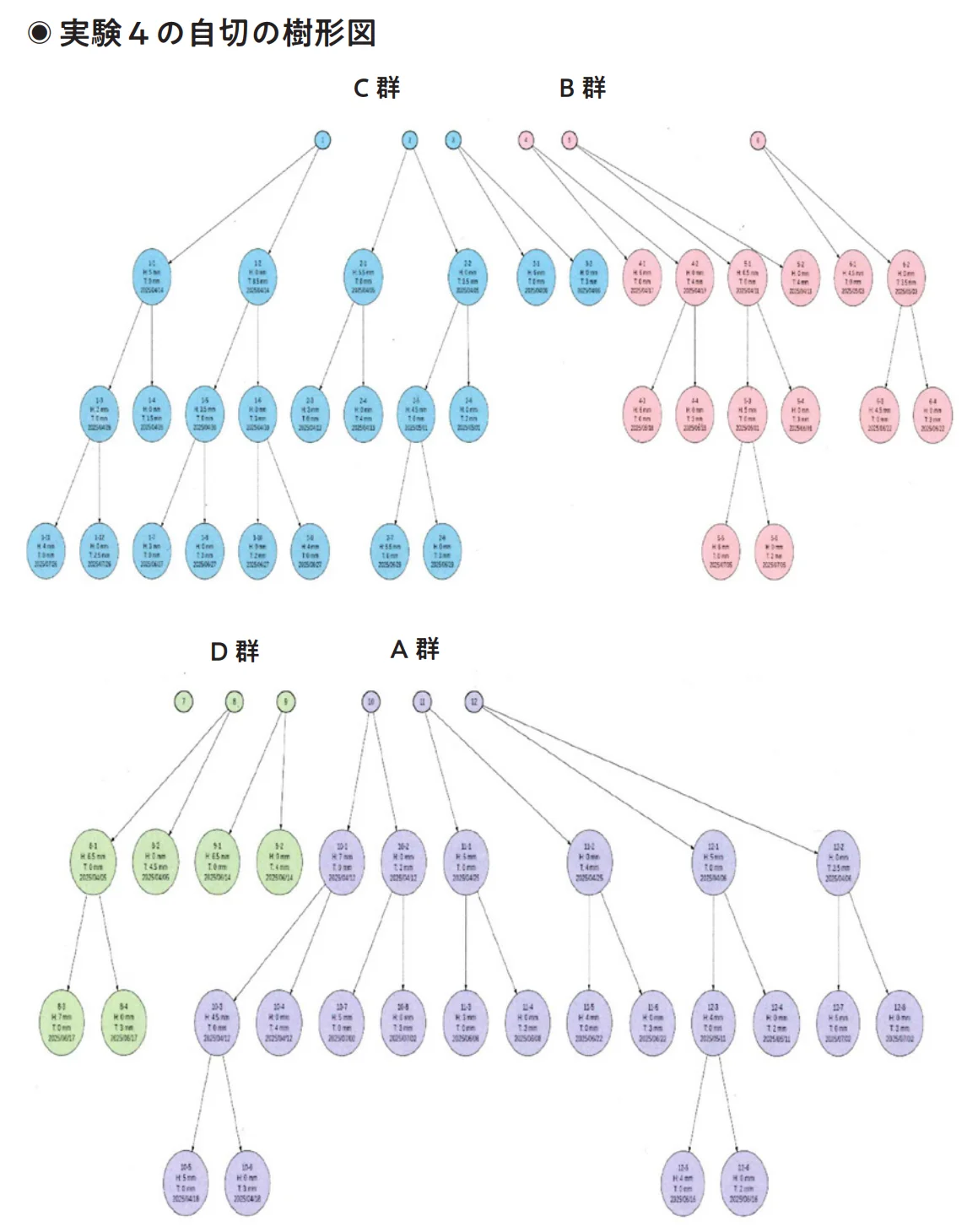
上の1〜3から伸びる樹形図は豚レバーだけのC群のもの、4〜6は豚レバー→赤虫のB群、下の7〜9は赤虫だけのD群、10〜12は赤虫→豚レバーのA群
実験4の結果が、上の図だ。最も自切が多かったのは、赤虫から豚レバーにエサを切り替えたA群だった。第3世代までは完璧に進み、第4世代まで進んだ個体もあった。豚レバーだけを与えたC群も自切が多く、第4世代まで進んだ個体は最も多かった。それに続くのが豚レバーから赤虫に切り替えたB群、最も自切が少なかったのは赤虫だけを与えたD群で、第3世代までしか進まなかったのに加え、1個体は1回も自切をしなかった。自切した時のそれぞれの平均体長を比べるとやはり、豚レバーを食べていた群が短く、なかでも豚レバーだけの群が最も短いことがわかる。逆に赤虫だけの群は最も長い。
この結果からも、豚レバーに含まれるたんぱく質やビタミンなどの栄養素が細胞の働きを活発にし、再生の速度を高めたと推察できる。豚レバーを食べた群は自切回数は多いが、自切するたびに小型化していき、赤虫だけの群は長さを保って着実に成長を続けている。赤虫だけの群がなぜ長い体を保ちながら成長できるのか、研究⑤では遺伝子の働きの違いを調べて明らかにしたい。

12穴プレートでの観察の様子
研究⑤
研究⑤では、RNA-seq(RNAシーケンス)という手法を使い、プラナリアの遺伝子発現を解析する実験を行った。RNAはリボ核酸と呼ばれ、生物の体内にある核酸という分子の一種。体の設計図である遺伝子情報は細胞内にある核のなかに、二重らせん構造のDNA(デオキシリボ核酸)として入っている。DNAの情報をもとにたんぱく質が作られ、できあがったたんぱく質の違いでその生物の最終的な体の形や機能が決まる。RNAにはDNAをもとにたんぱく質が作られる時、遺伝子情報やたんぱく質の材料を運んだり、たんぱく質工場の部品になったり、遺伝子の働きを調節したりする役目がある。
今回のRNA-seqは、まずプラナリアからRNAを抽出するところから始めた。次に、蛍光色素薬を混ぜ光を測る方法で、取り出したRNAの量や質を調べる。調べた後にRNAからDNAを合成する働きのある逆転写酵素を使い、RNAをDNAに換えて解析に使うサンプルを作った。作ったサンプルを、次世代シーケンサー(遺伝子の配列を短時間で調べられる装置、数百万の断片を一度に読み取ることができる)で解析する。この解析には、東邦大学理学部の鹿島誠教授の協力をいただいた。
解析から明らかになった各遺伝子の発現量からバイオリンプロットを作成し、さらに詳細に傾向を調べた。
実験5
実験を始めた2025年7月28日、冷凍赤虫だけを食べ続けていたプラナリア110匹を2つの群に分け、50匹には冷凍赤虫を与え続け、60匹には冷凍豚レバーを与えた。実験開始日から7日間(7月28〜31日、8月1日、4〜5日)、それぞれの群からプラナリアを8匹ずつ選び、RNAを抽出した。60匹の群に豚レバーを与えたのは、実験開始日の7月28日と、7月31日、8月3日だった。
最終的にRNA解析の結果が届いたのは、2カ月以上がたった10月9日だ。解析結果から、豚レバー群では再生や代謝に関わる遺伝子の発現が高いことがわかった。幹細胞の活性を示すpiwiや、細胞間の連絡を担うinx群、脂質代謝を調整するhnf4などの発現が特に高い。筋肉形成や組織再構築に関わる遺伝子の発現も高く、豚レバー群でより活発な成長、修復が進んでいることが示された。
赤虫群ではp53、xbp1など、細胞の安定化やストレス応答に関わる遺伝子の発現がやや高く、体を安定した状態に保つ遺伝子が働いていると考えられた。
この結果から、エサの違いは再生力に違いを生じさせる一因になる、と考えられる。

まとめと感想
この研究を通して、プラナリアがどんな栄養を使って体を再生させるのか、仕組みの一部が理解できた。今後はRNA-seqの結果をさらに詳しく調べ、どの遺伝子がどんな条件で働くのか、突き止めたい。研究を続けることで、将来の「人の再生医療」にもつながると思っている。
研究は大変なことも多かったが、変化に気づけたり、うまくいかないことから新しい発見もあったりして楽しかった。この研究を進められたのは、プラナリアたちのおかげである。プラナリアへの感謝と敬意を忘れずに、人のために役立つ研究を進めていきたい。
[審査員] 小澤 紀美子
文部科学大臣賞の受賞おめでとうございます。目の不自由な方との交流を通して発想したテーマ「もし、人間の目を再生出来たら多くの人々を幸せにできる」という視点での取り組み、とても興味深く作品を読ませていただきました。日本免疫学会主催の「免疫ふしぎ未来2024」に参加しながら専門家の力を自らの土俵に引き付けて、課題探究していく姿勢は小学生と思えないほどであり、すでに未来の科学者としての基本的能力を備えていると感嘆しました。プレ実験として冷凍豚レバーと冷凍赤虫の2種類のエサによる個体数の自切の変化を観察し、プラナリアの体長と自切の起こり方の違いを押さえたうえでエサの栄養の豊富さによる再生の違いを明らかにしています。こうした再生の実態を踏まえて、次の実験ではRNA解析による遺伝子の働き(発現)の違いを明らかにする段階へと実験を進めていき、プラナリアの体の大きさやRNA量の個体差を反映していると考察し、RNAは次の逆転反応やRNA-Seqライブラリー作成の十分な品質を備えていることを確認していく実験・研究プロセスは既に科学者としての資質を十分に証明していることを審査員一同高く評価しました。






















東邦大学理学部生物分子科学科 講師 鹿島 誠
佐藤君から初めて研究の相談を受けたのは小学3年生の時でしたが、実際に会い、その知的好奇心と研究姿勢に強い衝撃を受けました。分からないことを率直に問い、聞いた話を自分の疑問へ結びつける姿勢は、プロの研究者顔負けです。雑談の中で彼から餌を変えるとプラナリアがよく自切すると聞き、半信半疑ながら再現実験を提案したところ、餌依存的に自切頻度が増加する結果が得られました。その後、大学研究室での再実験では自切が再現されず困難に直面しましたが、その夜、「あきらめきれないので遺伝子発現解析をぜひやらせてください」とメールで直談判してきました。この熱意に心を動かされ解析を行った結果、餌によって遺伝子発現状態が変化することが明らかになりました。議論からヒントを得て、生成AIを活用しながら自ら問いを深めるという彼の姿勢は、今後の研究指導の受け方の一つのモデルであり、研究への情熱こそが原動力であると改めて実感しています。